toh
Troubles spéciaux
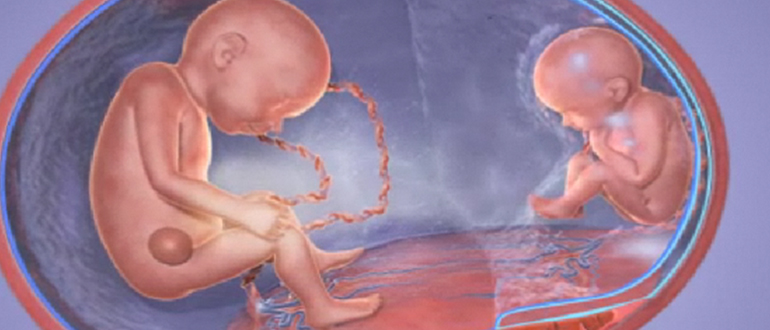 Les jumeaux monozygotes peuvent être atteints du syndrome transfuseur-transfusé. Le problème est situé au niveau des vaisseaux sanguins. Certains vaisseaux partent de chaque bébé, passent dans le cordon ombilical et se rendent jusque dans le placenta, où ils sont reliés entre eux. Ces vaisseaux sanguins spéciaux (appelés anastomoses) transportent le sang dans une seule direction. Un fœtus devient ainsi donneur de sang pour l’autre fœtus (le receveur). Cette situation peut créer un déséquilibre dans la quantité de liquide amniotique (vu à l’échographie) dans le sac amniotique de chaque bébé. Le fœtus receveur a trop de liquide amniotique (hydramnios), tandis que le fœtus donneur diminue presque complètement sa production de liquide amniotique jusqu’au point où il finit par en manquer (oligoamnios). Ce syndrome apparaît souvent au deuxième trimestre, mais il peut être dépisté même au début du troisième trimestre. Il y a plusieurs stades possibles. Si votre médecin dépiste ce syndrome lors d’une échographie, il pourra recommander un traitement pour interrompre la circulation de sang entre les fœtus. Ce traitement, réalisé par laser, permet de bloquer les vaisseaux problématiques. Il est offert à l’Hôpital Mount Sinai de Toronto. Après le traitement, vous irez à de fréquents rendez-vous de suivi à L’Hôpital d’Ottawa jusqu’à la naissance de vos bébés.
Les jumeaux monozygotes peuvent être atteints du syndrome transfuseur-transfusé. Le problème est situé au niveau des vaisseaux sanguins. Certains vaisseaux partent de chaque bébé, passent dans le cordon ombilical et se rendent jusque dans le placenta, où ils sont reliés entre eux. Ces vaisseaux sanguins spéciaux (appelés anastomoses) transportent le sang dans une seule direction. Un fœtus devient ainsi donneur de sang pour l’autre fœtus (le receveur). Cette situation peut créer un déséquilibre dans la quantité de liquide amniotique (vu à l’échographie) dans le sac amniotique de chaque bébé. Le fœtus receveur a trop de liquide amniotique (hydramnios), tandis que le fœtus donneur diminue presque complètement sa production de liquide amniotique jusqu’au point où il finit par en manquer (oligoamnios). Ce syndrome apparaît souvent au deuxième trimestre, mais il peut être dépisté même au début du troisième trimestre. Il y a plusieurs stades possibles. Si votre médecin dépiste ce syndrome lors d’une échographie, il pourra recommander un traitement pour interrompre la circulation de sang entre les fœtus. Ce traitement, réalisé par laser, permet de bloquer les vaisseaux problématiques. Il est offert à l’Hôpital Mount Sinai de Toronto. Après le traitement, vous irez à de fréquents rendez-vous de suivi à L’Hôpital d’Ottawa jusqu’à la naissance de vos bébés.
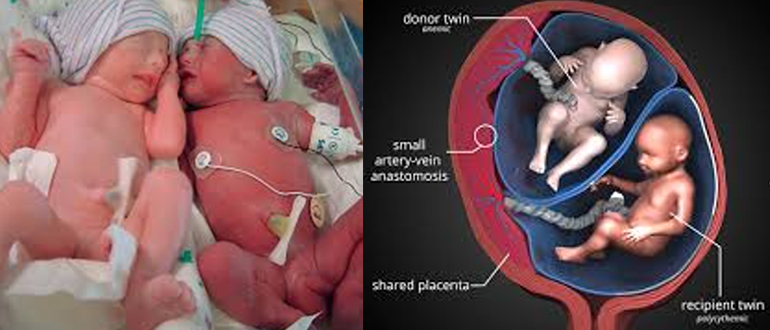 La séquence anémie-polycythémie est un autre trouble propre aux jumeaux monozygotes causé par une lente transfusion de sang d’un fœtus à l’autre. Comme dans le cas du syndrome transfuseur-transfusé, il est dû à la présence de vaisseaux sanguins communicants dans le placenta, mais ces vaisseaux sont habituellement plus petits et moins nombreux que dans le cas du syndrome transfuseur-transfusé. Le problème fait en sorte qu’un des bébés peut devenir très anémique pendant que l’autre peut avoir le sang épais et un taux d’hémoglobine élevé. Aucune de ces situations n’est bonne à long terme. Heureusement, ce trouble survient spontanément dans seulement 5 % des cas de jumeaux monozygotes. Il survient plus souvent (environ 11 % des cas) après le traitement par laser du syndrome transfuseur-transfusé s’il reste toujours de très minuscules vaisseaux sanguins communicants (d’un calibre d’environ 1 mm). Le traitement peut comprendre une transfusion de sang avant la naissance (intra-utérine) pour résoudre l’anémie du bébé et accroître son apport en oxygène. Il pourra aussi être nécessaire de retirer une partie du sang épaissi pour le remplacer par une solution saline chez l’autre jumeau.
La séquence anémie-polycythémie est un autre trouble propre aux jumeaux monozygotes causé par une lente transfusion de sang d’un fœtus à l’autre. Comme dans le cas du syndrome transfuseur-transfusé, il est dû à la présence de vaisseaux sanguins communicants dans le placenta, mais ces vaisseaux sont habituellement plus petits et moins nombreux que dans le cas du syndrome transfuseur-transfusé. Le problème fait en sorte qu’un des bébés peut devenir très anémique pendant que l’autre peut avoir le sang épais et un taux d’hémoglobine élevé. Aucune de ces situations n’est bonne à long terme. Heureusement, ce trouble survient spontanément dans seulement 5 % des cas de jumeaux monozygotes. Il survient plus souvent (environ 11 % des cas) après le traitement par laser du syndrome transfuseur-transfusé s’il reste toujours de très minuscules vaisseaux sanguins communicants (d’un calibre d’environ 1 mm). Le traitement peut comprendre une transfusion de sang avant la naissance (intra-utérine) pour résoudre l’anémie du bébé et accroître son apport en oxygène. Il pourra aussi être nécessaire de retirer une partie du sang épaissi pour le remplacer par une solution saline chez l’autre jumeau.
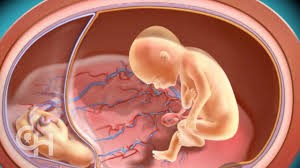 Le retard de croissance intra-utérin sélectif touche environ 15 % des jumeaux monozygotes. Il y a habituellement une différence significative (écart) dans le poids estimé des jumeaux selon l’évaluation par échographie. Un des fœtus aura aussi un poids estimé inférieur au 10e percentile. C’est-à-dire que plus de 90 % des jumeaux monozygotes auront un poids (estimé par échographie) supérieur à celui du bébé plus petit. Contrairement à ce qui est observé dans le cas du syndrome transfuseur-transfusé, il n’y a habituellement pas de grande différence dans le volume de liquide amniotique autour de chaque bébé. Le médecin qui soupçonne un retard de croissance examinera attentivement la circulation sanguine dans les artères des cordons ombilicaux. Différents modèles de circulation sanguine ont été associés à des différences dans les taux de survie et l’âge gestationnel à la naissance.
Le retard de croissance intra-utérin sélectif touche environ 15 % des jumeaux monozygotes. Il y a habituellement une différence significative (écart) dans le poids estimé des jumeaux selon l’évaluation par échographie. Un des fœtus aura aussi un poids estimé inférieur au 10e percentile. C’est-à-dire que plus de 90 % des jumeaux monozygotes auront un poids (estimé par échographie) supérieur à celui du bébé plus petit. Contrairement à ce qui est observé dans le cas du syndrome transfuseur-transfusé, il n’y a habituellement pas de grande différence dans le volume de liquide amniotique autour de chaque bébé. Le médecin qui soupçonne un retard de croissance examinera attentivement la circulation sanguine dans les artères des cordons ombilicaux. Différents modèles de circulation sanguine ont été associés à des différences dans les taux de survie et l’âge gestationnel à la naissance.
La perte d’un jumeau monozygote est plus fréquente que la perte d’un jumeau dizygote. Parfois, c’est clairement lié à l’un des troubles qui touchent spécifiquement les jumeaux monozygotes. Bien des fois, la perte est imprévue et imprévisible, même avec une surveillance intensive par échographie et des rendez-vous de suivis toutes les deux semaines tout au long de la grossesse. Selon les estimations, le taux de perte d’un ou deux fœtus monozygotes après la 34e semaine peut atteindre jusqu’à 4 % malgré une surveillance intensive. La seule stratégie permettant de prévenir cet événement indésirable est de mettre au monde tous les jumeaux monozygotes de façon prématurée à la 34e semaine. Or, si cette stratégie devenait une norme de soins, il y aurait beaucoup plus de problèmes associés à la prématurité et nos pouponnières de soins intensifs déborderaient. Pour favoriser la survie des fœtus vers la fin de la grossesse, nous choisissons de mettre au monde les jumeaux monozygotes vers la 36e semaine en assurant une surveillance intense jusqu’à ce moment.
Si un jumeau monozygote décède dans l’utérus, le risque de décès de l’autre jumeau est de 12 %. Le décès du premier jumeau peut aussi entraîner d’importants problèmes de développement neurologique au second jumeau en raison d’un transfert de sang du jumeau survivant vers le jumeau décédé. Cela diminue la circulation sanguine dans le cerveau du jumeau survivant et provoque une atteinte au cerveau dans environ 30 % des cas. La gravité de cette conséquence varie selon le moment de la perte. Elle est plus susceptible d’être problématique si elle survient vers la fin du deuxième ou du troisième trimestre. Si un fœtus décède au début de la grossesse, on ne recommandera pas nécessairement la mise au monde prématurée de l’autre fœtus parce que les dommages potentiels au survivant se produisent au moment de la perte.
La séquence de perfusion artérielle inversée est un trouble très rare chez les jumeaux monozygotes. Il survient dans seulement environ 1 grossesse sur 35 000. Un fœtus se développe normalement tandis que l’autre présente de graves différences structurelles. Le bébé ayant une structure normale (souvent appelé le jumeau pompe) envoi du sang vers l’autre fœtus (souvent appelé le jumeau perfusé). Son cœur travaille donc beaucoup plus fort que la normale pour soutenir son jumeau.
Du sang faible en oxygène et riche en déchets est pompé d’un bébé vers l’autre par une seule artère qui les relie. Le bébé qui reçoit le sang faible en oxygène ne se développe pas normalement. Vu qu’il lui manque une structure cardiaque, il dépend entièrement de son jumeau pour assurer sa survie. Le jumeau pompe peut alors devenir atteint d’insuffisance cardiaque. Si votre médecin diagnostique ce trouble, il vous expliquera plusieurs options pour améliorer la chance de survie du jumeau pompe. Les différences structurelles chez le jumeau perfusé sont graves et incompatibles avec la vie.
Les jumeaux conjoints, aussi parfois appelés jumeaux siamois, sont très rares. Avec le recours au dépistage par échographie au cours du premier trimestre, ils sont souvent détectés au début de la grossesse. Dans les cas les plus graves, les fœtus partagent des structures comme le cœur ou le foie, ce qui rend leur séparation après la naissance très difficile, voire impossible. Les complications liées à la grossesse, par exemple la perte de fœtus ou l’accouchement prématuré, sont également fréquentes dans ces cas. Le succès d’une tentative de séparation, lorsque possible, dépend de nombreux facteurs et nécessite une évaluation détaillée par de nombreuses spécialités différentes. Ces grossesses sont donc évaluées à Toronto.
Page mise à jour le 29 avril 2021


 To reset, hold the Ctrl key, then press 0.
To reset, hold the Ctrl key, then press 0.